La tabla periódica nace de la necesidad que tuvieron los científicos de ordenar los elementos químicos descubiertos a través de los años, es así como gracias a los aportes que cada uno realizó podemos observar este ordenamiento cuya base son las propiedades de cada uno de los elementos. Llegar a lograr la actual tabla periódica fue un gran desafío que conllevó un sin número de errores, pero gracias a la perseverancia y el trabajo constante de los diferentes científicos se logró llevar a cabo.
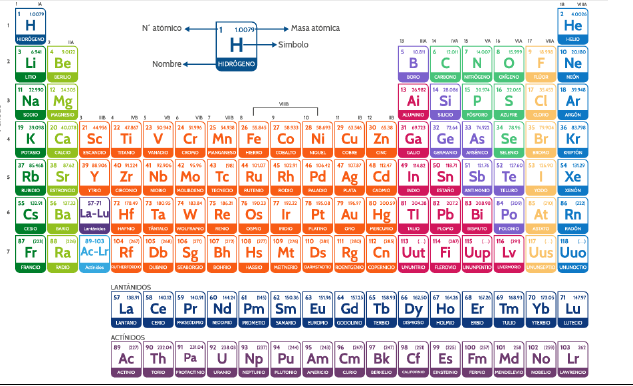
HISTORIA DE LA TABLA PERIÓDICA
Aportes de los Científicos. El descubrimiento de un gran número de elementos indujo a los químicos a buscar una clasificación para ellos, de acuerdo a similitudes en sus propiedades químicas y físicas, con el objeto de facilitar su conocimiento y su descripción sistémica en función de sus analogías y diferencias, lo cual generó la tabla periódica moderna que conocemos.
La tabla periódica en cualquiera de sus formas es una representación racional y sistémica de las propiedades de los elementos químicos, y su fundamento es la ley periódica.
La primera definición científica de elemento químico fue establecida por:
Robert Boyle en 1661: sustancia simple. Sin embargo, 100 años después Lavoisier todavía incluía en la lista de elementos a la luz y al calórico, que se suponía que era una especie de fluido que transportaba al calor.
•Döbereiner – 1828: Notó que existían grupos de tres elementos que tenían propiedades químicas semejantes y que sus propiedades físicas variaban de manera ordenada de acuerdo con sus masas atómicas. A estas series las llamó triadas.
•Chancourtois -1962: Fue el primero en arreglar los elementos químicos según su peso atómico (masa atómica). Construyo una hélice de papel en la que estaban ordenados los elementos por pesos atómicos, poniendo en evidencia una cierta periodicidad entre los elementos de la tabla.
•Newlands – 1863: Ordenó a los elementos con base en sus masas atómicas y observó que cada octavo elemento tenía propiedades semejantes al primero. Este hecho fue nombrado la ley de las octavas, pero no se cumplía con elementos de mayor masa atómica, por lo que fue rechazada.
•Mendeléiev – 1869: Propuso clasificar a los elementos de acuerdo con la repetición regular y periódica de sus propiedades. Su propuesta superó a la de Newlands, porque la agrupación de los elementos de acuerdo con sus propiedades fue exacta, además dejó espacios vacíos prediciendo la existencia de elementos hasta entonces desconocidos.
•Meyer – 1869: Su clasificación de los elementos coincidió con la Mendeléiev, aunque eran de países diferentes, él de Alemania y Mendeléiev de Rusia.
•Moseley – 1913: Descubrió que el número atómico aumenta en el mismo orden que la masa atómica periódica.
•Seaborg – 1944: Descubrió y aisló 10 elementos químicos transuránicos, elementos con número atómico superior a 92. Además, fue el primero en proponer la serie actínida, que contribuyó a la clasificación actual de la tabla periódica.
CLASIFICACIÓN DE LOS ELEMENTOS QUÍMICOS
La tabla periódica moderna se basa en la configuración electrónica, la cual logra explicar la repetición de propiedades físicas y químicas. Los elementos químicos pueden clasificarse según diferentes criterios, los más comunes los veremos a continuación:
•
Clasificación según configuración electrónica externa (estructura electrónica). Dentro de un mismo grupo se encuentran solo elementos con igual configuración electrónica externa, es decir, finales de configuración que solo varían en el valor de n (periodos). De este modo, los elementos de un grupo de la tabla periódica comparten la ubicación de sus últimos electrones.
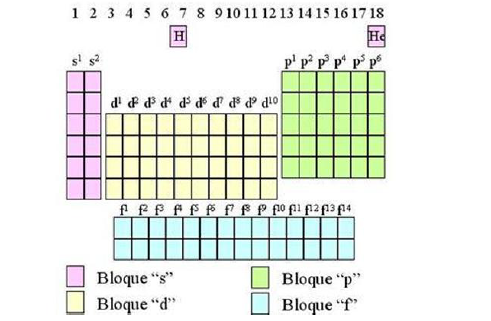
• Clasificación según propiedades estructurales y eléctricas.
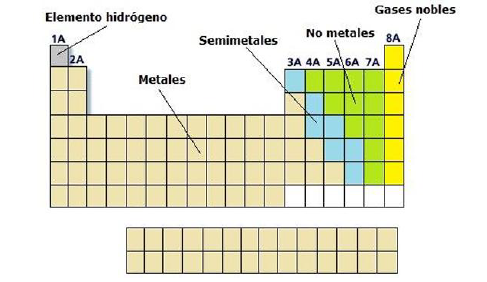
Las propiedades estructurales y eléctricas de los elementos derivan de su comportamiento frente a los electrones. De esta forma tenemos:
Metales: Son elementos con tendencia a ceder fácilmente electrones para formar cationes, baja energía de ionización, baja afinidad electrónica, baja electronegatividad, Forman compuestos con los no metales y no con los metales, son buenos conductores del calor y la electricidad, tienen brillo, son dúctiles, maleables, y tienen alto punto de fusión.
No metales: Son elementos con tendencia a ganar electrones para formar aniones, elevada energía de ionización, elevada electronegatividad, Forman compuestos con los metales, son malos conductores de calor y electricidad, tiene propiedades de aislante; No tienen brillo, tienen bajo punto de fusión y ebullición.
Metaloides: también llamados anfóteros significa que actúa como ácido o como base según la sustancia con que reacciona, son elementos que presentan tendencias intermedias entre los metales y los no metales.
Propiedades periódicas: Las propiedades periódicas de los elementos químicos, son características propias de dichos elementos que varían de acuerdo a su posición en la tabla periódica, ósea dependiendo de su número atómico. Las propiedades periódicas son: electronegatividad, radio atómico, afinidad electrónica, potencial de ionización, radio iónico, el volumen atómico, carácter metálico, carga nuclear efectiva, temperatura de fusión y temperatura de ebullición.
Radio atómico: Los radios atómicos se basan en la distancia promedio del núcleo a la capa más externa del átomo. El elemento con mayor radio atómico es el Francio “Fr” El radio atómico varía así: en un período: aumenta de derecha a izquierda y en un grupo: aumenta de arriba hacia abajo.
• Afinidad electrónica: Es la energía liberada cuando un átomo gaseoso capta un electrón y se convierte en un anión. En un período aumenta de izquierda a derecha y en un grupo aumenta de abajo hacia arriba.
• Potencial o energía de ionización: Es la energía mínima necesaria para arrancar un electrón de un átomo gaseoso. En un periodo aumenta de izquierda a derecha y en un grupo aumenta de abajo hacia arriba. Los gases nobles son los elementos de MAYOR potencial de ionización.
• Electronegatividad: es la capacidad que tienen los átomos para atraer electrones. En un periodo aumenta de izquierda a derecha y en grupo aumenta de abajo hacia arriba. Elemento más electronegativo de la tabla periódica es el Fluor “F”.
• Carácter metálico: Capacidad de un elemento para perder electrones. En un periodo aumenta de derecha a izquierda y en un grupo aumenta de arriba hacia abajo. La familia más metálica son los alcalinos y el elemento más metálico es el francio.
• Volumen atómico: Se define como el cociente entre la masa atómica y la densidad. Al igual que el radio atómico, en un grupo aumenta hacia abajo (↓), y en un período aumenta de derecha a izquierda.
En la siguiente figura se tiene el resumen de cómo es la tendencia de aumento de las propiedades periódicas con respecto a los períodos y grupos en la tabla periódica.
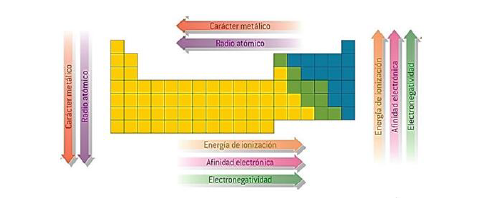
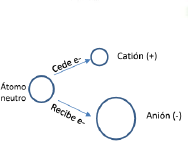
Radio iónico: corresponde al radio que alcanza un átomo luego de haber sufrido una ganancia o pérdida de electrón.
Cationes: tienen carga positiva, se forman cuando el átomo neutro pierde electrones. Los elementos que ceden sus electrones son los metálicos, los grupos 1 y 2 de la tabla periódica.
Aniones: tienen carga negativa, se forman cuando el átomo neutro gana electrones. Los elementos que reciben electrones son los no metales, los grupos 16 y 17 de la tabla periódica.
La tabla periódica moderna: está organizada por 7 períodos y 18 grupos.
•Los períodos: están representados por las filas de la tabla. Son 7 períodos horizontales. El número del período coincide con el número de niveles que tiene el átomo en su configuración electrónica.
•Los Grupos: Son las columnas de la tabla. Son 18 grupos verticales que contienen a elementos de la misma familia. En ellos coincide la terminación de la configuración electrónica, es decir coinciden en la forma del último subnivel, en la cantidad de electrones en su último subnivel.
•Los grupos de la Tabla Periódica se dividen en Familias:
Familia “A”: Elementos representativos
Familia “B”: Elementos de transición
Familia a. Elementos representativos:
•Familia IA: De los alcalinos, comprenden los elementos del grupo 1, desde el Li hasta el Fr, todos son metales, suaves y brillantes. N° de oxidación +1, tienen un electrón de valencia. Su configuración electrónica termina en ns1.
Familia IIA: De los alcalino-térreos, comprende los elementos del grupo 2 desde el Be hasta el Ra, todos son metales N° de oxidación +2, tiene 2 electrones de valencia. Su configuración electrónica termina en ns2.
• Familia IIIA: De los térreos. Comprende los elementos del grupo 13, desde el B hasta el Tl, el Boro es un no metal, los demás son metales. N° de oxidación +3, 3 electrones de valencia. Su configuración electrónica termina en ns2 np1.
•Familia IVA: Del carbono o carbonaideos, Comprende los elementos del grupo 14 desde el C hasta el Pb, el C y el Si son no metales, los demás son metales. N° de oxidación +2,+4,-4, 4 electrones de valencia. Su configuración electrónica termina en ns2 np2.
•Familia VA. De nitrógeno o nitrogenoideos. Comprende los elementos del grupo 15, desde el N hasta el Bi, el N, P y el As son no metales, los demás son metales. N° de oxidación +3,+5,-3, 5 electrones de valencia. Su configuración electrónica termina en ns2 np3.
•Familia VIA: Calcógenos o de Oxígenos. Comprende los elementos del grupo 16 desde el O hasta el Po. El Po es un metal, los demás son no metales. N° de oxidación +2,+4,+6 y -2, Oxígeno (-1 y-2), 6 electrones de valencia. Su configuración electrónica termina en ns2 np4.
•Familia VIIA: Halógenos. Comprende los elementos del grupo 17 desde el F hasta el At, todos son no metales, forman moléculas diatómicas. N° de oxidación +1,+3,+5,+7 y -1, el F sólo -1. F, Cl, I son gases, Br, liquido, At sólido.7 electrones de valencia. Su configuración electrónica termina en ns2 np5.
•
Los gases nobles: Ocupan la última columna de la derecha de la tabla, son los elementos del grupo 18, no tienen actividad química (no ganan ni pierden electrones) es por eso que su valencia es cero, esto se debe a que tienen en su configuración 8 electrones en su último nivel, con excepción del helio que tiene dos; existen como átomos no como moléculas y son He, Ne, Ar, Kr, Xe y Ra. Su configuración electrónica termina en ns2 np6.
•Elementos de transición. Son los elementos que pertenecen a la familia B, están situados en la parte central del sistema periódico, pertenecientes a los grupos 3 al 12, su configuración electrónica termina en los orbitales “d”. Su nombre proviene de una característica que presentan estos elementos de poder ser estables por si mismo sin necesidad de una reacción con otro elemento. Todos son metales. Su configuración electrónica es (n-1) dx n s2 (x= 1, 2, …, 10).
•Elementos de transición interna: antiguamente eran conocidos como tierras raras, los forman dos series, una Lantánidos comienza en el Lantano (Z=57) y termina en Lutecio (Z= 71) y la otra Actínidos comienza en Actinio (Z= 89) y termina en el Laurencio (Z= 105), A los lantánidos y actínidos se les conoce como elementos de transición interna. Su configuración electrónica termina en los orbitales “f”. Su configuración electrónica es (n-2) fx (n-1) d0 n s2 (x= 1, 2, …, 14)
Actividad 1.
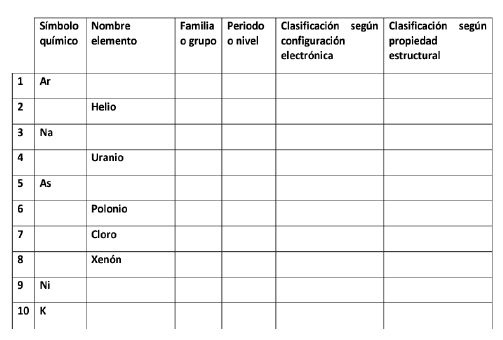
1. Con la información aquí entregada y la ayuda de una tabla periódica completa la tabla que se encuentra a continuación, donde debes clasificar cada uno de los elementos expuestos.
2. Crea una línea de tiempo ordenando la historia de la Tabla periódica.
Completa la siguiente tabla con las indicaciones presentadas a continuación:
Según el grupo y periodo que se entrega, escriba en la tabla periódica el símbolo del elemento correspondiente:
a) Periodo 1 grupo 1 b) Periodo 2 grupo 14
c) Periodo 4 grupo 16 d) Periodo 5 grupo 5
e) Periodo 5 grupo 13 f) Periodo 6 grupo 15
Escriba en la tabla periódica el símbolo de los gases nobles
Escriba en la Tabla Periódica el Símbolo de los elementos que tienen los siguientes números Atómicos:
a) Z= 10 b) Z= 118
c) Z= 35 d) Z= 49
e) Z= 95 f) Z=77
g) Z= 29